2026.05.11
實體瘤的腫瘤微環境(TME)是製約T細胞療法療效的關鍵因素。該環境以低氧、低pH、多種抑製性信號(如細胞表面受體、代謝產物、脂質等)及高瘤內壓力為特征,會持續誘導浸潤的T細胞出現功能抑製、耗竭乃至死亡,嚴重限製TCR-T、CAR-T等T細胞免疫療法在實體瘤中的治療效果與療效的持久性。本研究旨在優化T細胞體外製備工藝,在細胞生產階段對治療性T細胞進行腫瘤微環境預適應馴化,提升其在惡劣腫瘤微環境中的存活能力與抗腫瘤功能。
研究團隊采用AVATAR Odyssey培養系統,在小規模非病毒基因編輯過程中精準調控氧濃度與壓力,使T細胞在製備階段接受類腫瘤微環境(TME)條件的預適應馴化。通過該方式,成功獲得經代謝重編程的TCR-T細胞,顯著提升其在低氧、高壓等惡劣TME條件下的適應性與抗腫瘤效能。
實驗設計:三組對照,精準對比馴化效果
研究依托AmplifyBio非病毒基因編輯平臺,構建靶向HPV-16 E7蛋白的特異性TCR-T細胞,並將其分為三組培養,重點對比不同環境下的細胞表現:
• 對照組:常氧常壓(常規培養箱,氧濃度約18.6%)
• 實驗組1:5% O₂/5 PSI(AVATAR系統精準調控)
• 實驗組2:1% O₂/5 PSI(AVATAR系統精準調控)
隨後通過細胞活力檢測、流式細胞術、海馬代謝分析、體外殺傷實驗、小鼠體內模型驗證等多項檢測,全面評估T細胞的增殖、代謝、功能等核心性能。
實驗結果
研究人員使用3名健康供體的PBMC構建HPV特異性TCR-T細胞,將其分別置於三組條件下擴增培養14天後,系統評估細胞的活力、增殖能力、表型特征、代謝水平、基因表達模式及體內外抗腫瘤功能。
1. 低氧高壓下TCR-T細胞保持高活力,適度低氧不影響擴增
兩組實驗組細胞活力與常氧對照組無顯著差異;5% O₂/5 PSI組細胞擴增倍數與常氧組相當;1% O₂/5 PSI組的總擴增倍數顯著下降,且CD8陽性T細胞的擴增倍數降低幅度更為顯著。
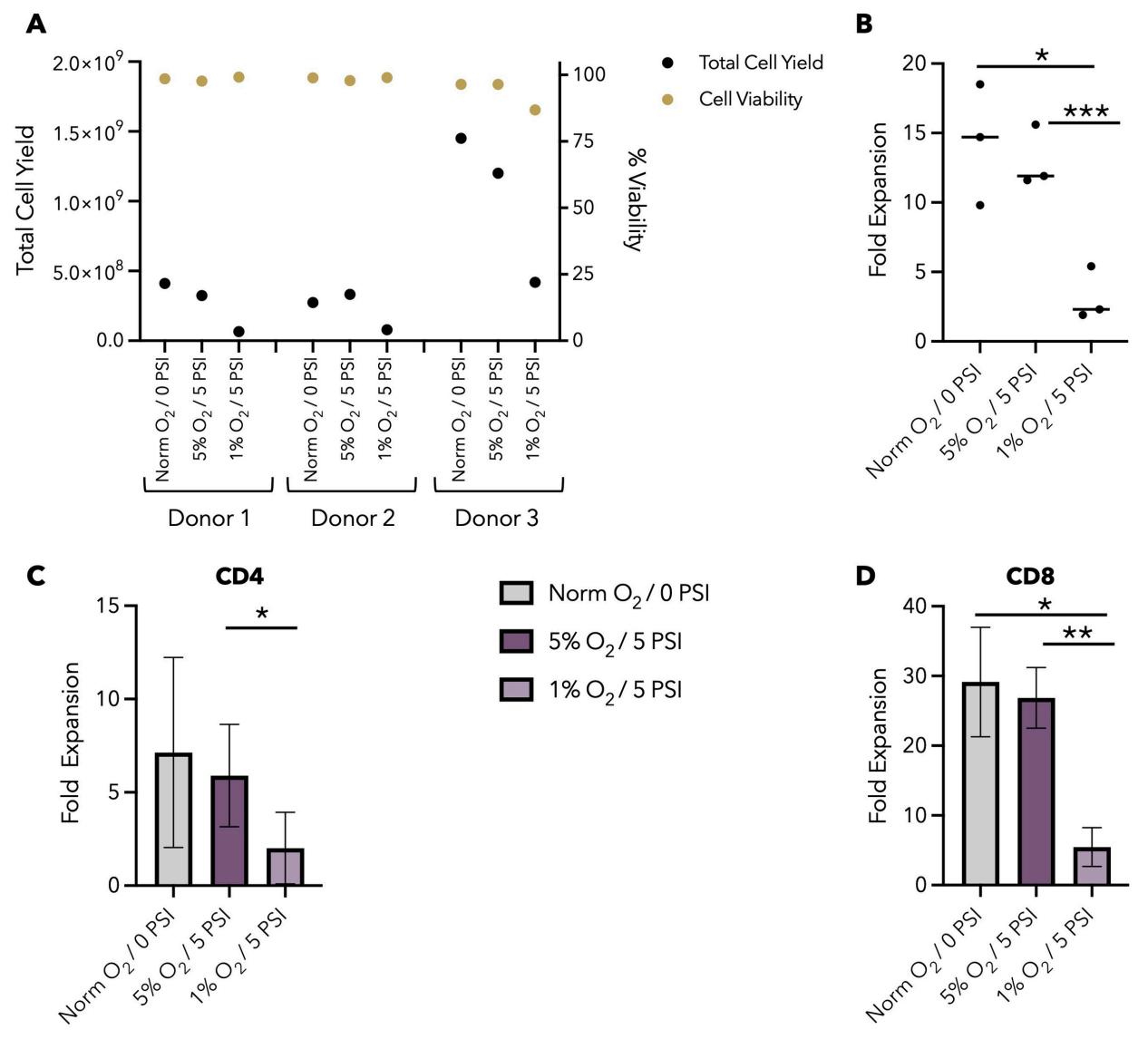
圖 1. 三種培養條件下 HPV 特異性 T 細胞的活力與擴增情況
2. TCR 編輯效率與記憶表型整體穩定
三種培養條件下TCR編輯效率相近(平均35%–45%),僅1% O₂/5 PSI組CD8陽性T細胞編輯效率略低。常氧組與5% O₂/5 PSI組中,絕大多數CD4與CD8陽性T細胞呈幹細胞樣記憶表型,兩組間無顯著差異;而1% O₂/5 PSI組的細胞表型則出現明顯改變。
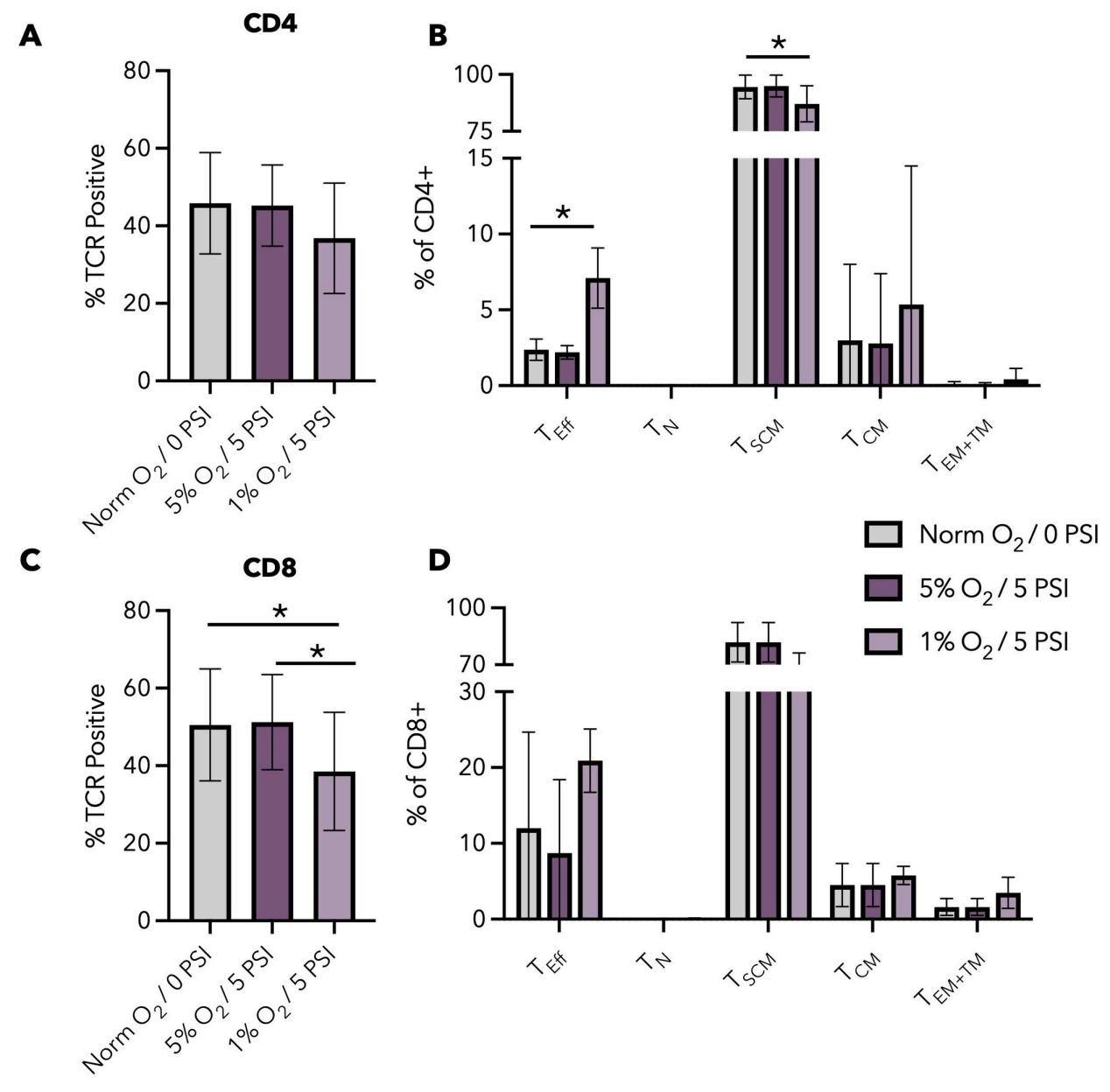
圖 2. 不同培養條件下 TCR 編輯效率及 T 細胞亞群分析
3. 耗竭表型整體較低,1% O₂/5 PSI 組 CD25、CD39 表達上升
三組 CD4⁺、CD8⁺T 細胞的耗竭標誌物(4-1BB、TIM-3、TIGIT、PD-1、LAG-3)表達水平均處於較低水平,未出現明顯功能耗竭;低氧條件與抑製性受體 TIM 3、TIGIT 以及低水平的 PD-1 表達升高相關,同時也與活化標誌物 CD25 及 TME 相關抗原 CD39 的表達升高相關。
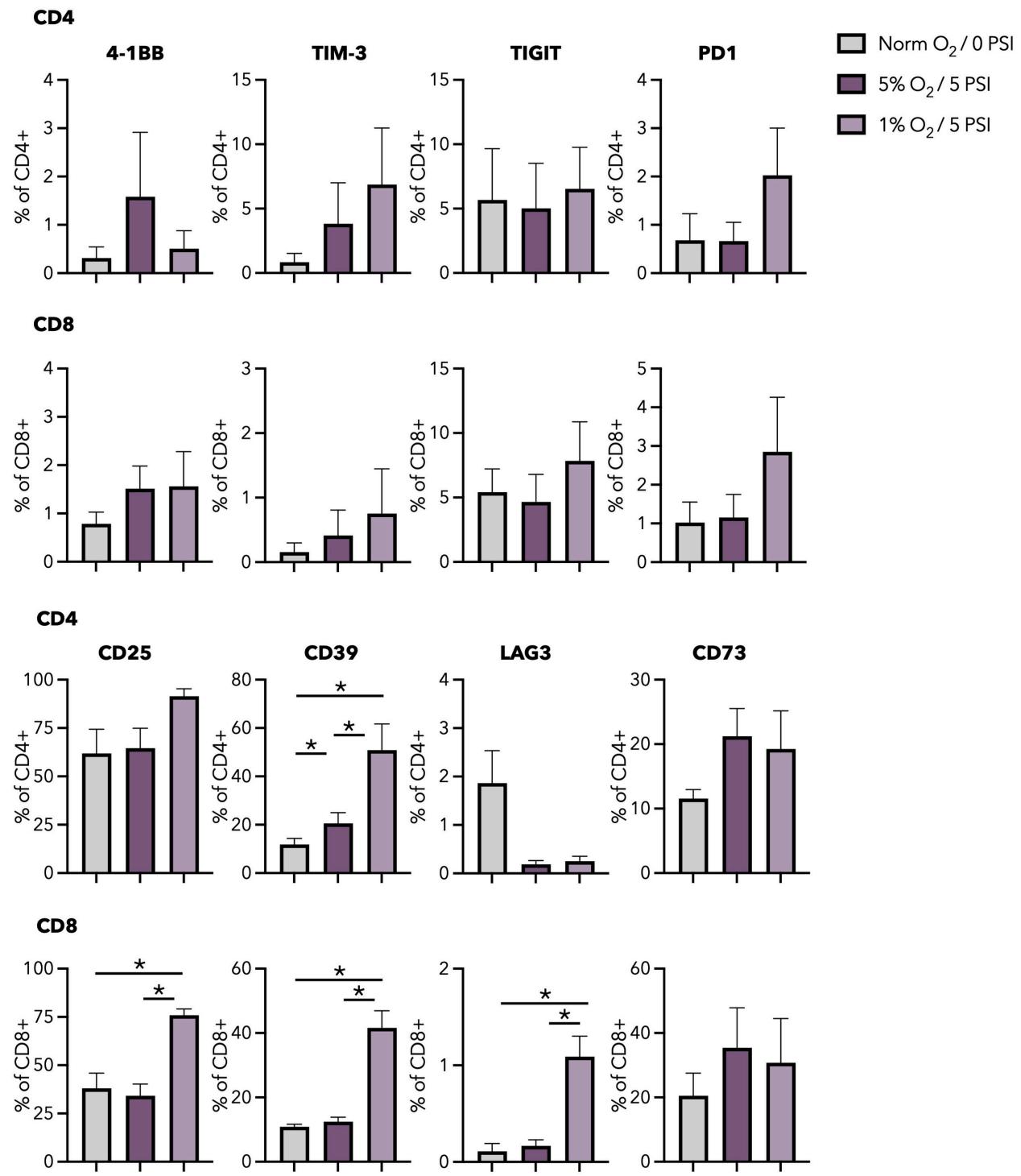
圖 3. 不同培養條件下 T 細胞表型特征分析
4. 5% O₂/5 PSI 條件誘導抗腫瘤炎癥基因特征
RNA測序顯示:5% O₂/5 PSI組低氧相關基因(HSF4、IGFBP2、VEGFA)、mTORC1信號通路、糖酵解通路顯著上調;同時IL-2、IFN-γ、TNF-α、IL-6等介導的抗腫瘤、促炎通路激活,提示細胞效應功能提升。1% O₂/5 PSI組低氧通路、糖酵解通路、細胞應激通路均上調,但IFN-γ通路下調。
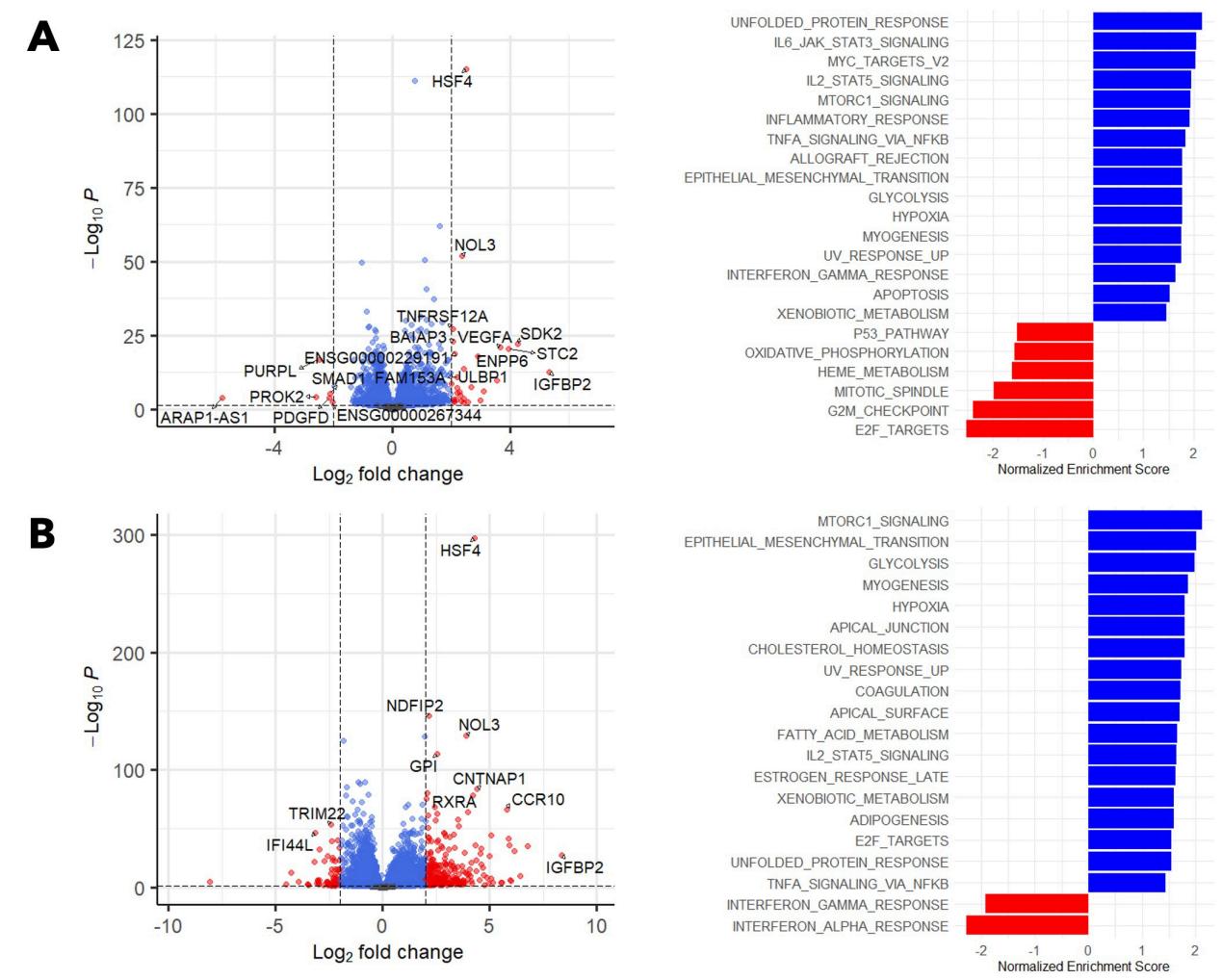
圖 4. 腫瘤微環境預處理相關的抗腫瘤炎癥基因表達特征
5. 5% O₂/5 PSI 組線粒體功能完整,呼吸儲備能力正常
海馬代謝分析顯示:常氧組與5% O₂/5 PSI組耗氧率(OCR)、備用呼吸能力(SRC)相當,線粒體功能正常;1% O₂/5 PSI組OCR與SRC顯著降低,呼吸與糖酵解潛能下降;5% O₂/5 PSI組細胞呈現出典型的低氧適應代謝特征——糖酵解依賴程度增強,同時線粒體功能得以完整保留。
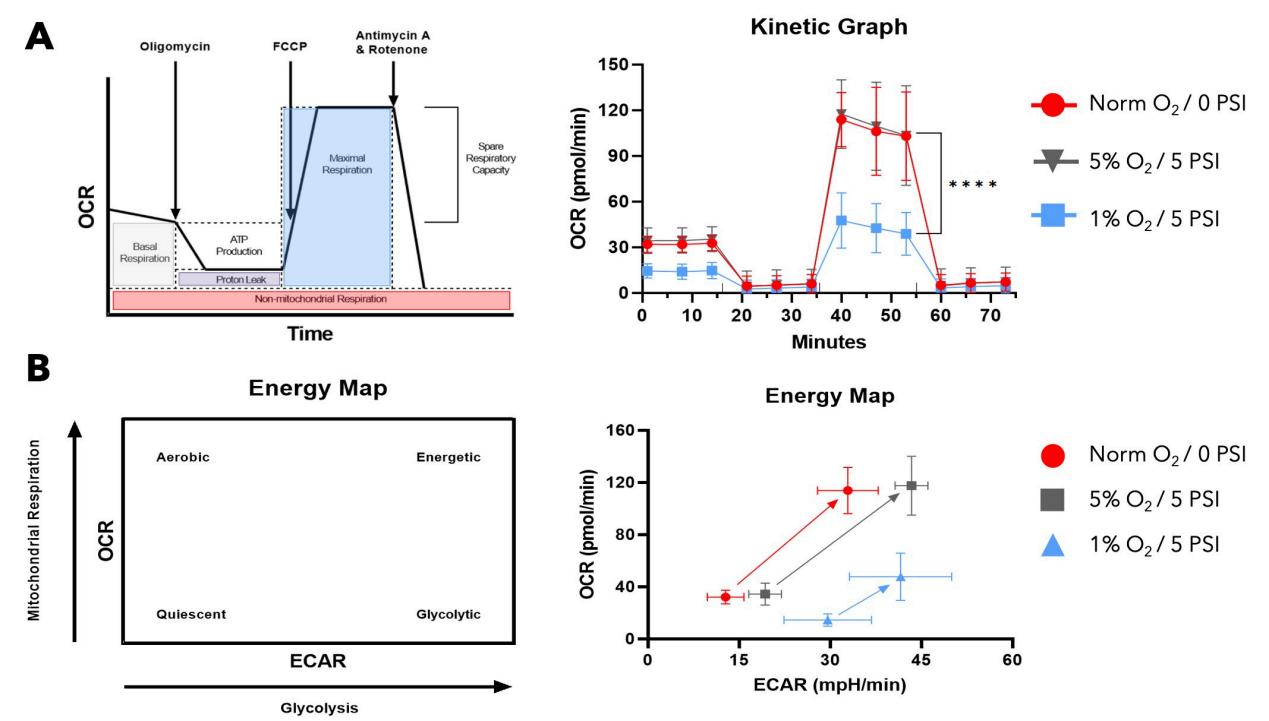
圖 5. 不同培養條件下 T 細胞的氧消耗與代謝表型變化
6. 5% O₂/5 PSI 組體外殺傷顯著增強,體內腫瘤控製效果穩定
體外殺傷實驗(模擬腫瘤微環境):5% O₂/5 PSI 組在低效靶比(1:30、1:50、1:100)下仍表現出更強的腫瘤殺傷能力,1% O₂/5 PSI 組殺傷效果最差; NOG 小鼠體內模型實驗:經5% O₂/5 PSI 馴化的 TCR-T 細胞,體內腫瘤控製效果與常氧組相當,且具備穩定的體內抑瘤能力。
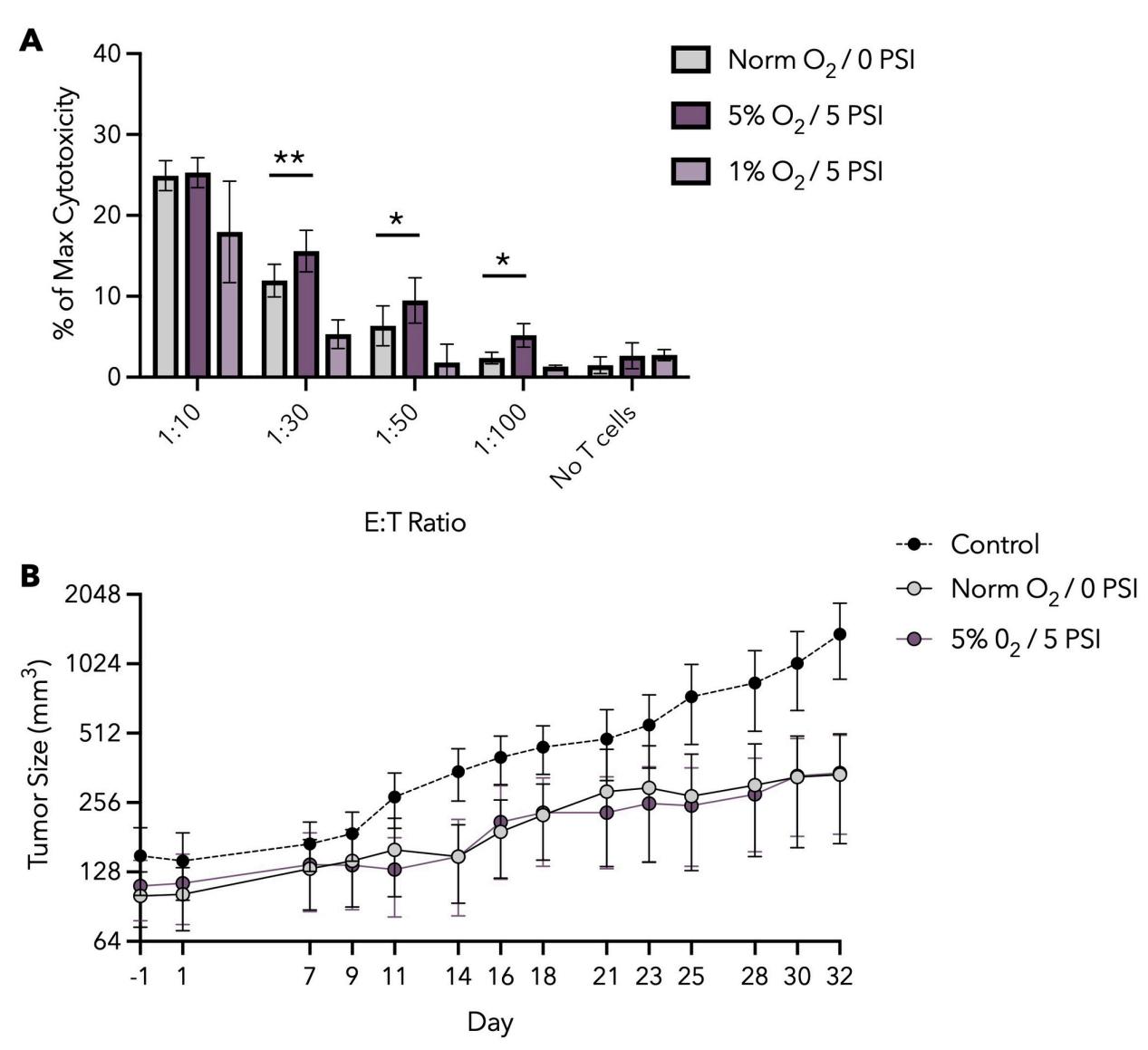
圖 6.TCR-T 細胞體外殺傷活性及體內腫瘤控製效果
實驗結論
本研究通過三組對照實驗證實,AVATAR Odyssey培養系統可在低氧/高壓類腫瘤微環境條件下穩定製備功能性HPV特異性TCR-T細胞,其中5% O₂/5 PSI是本研究條件下平衡細胞擴增與功能提升的最優預適應馴化條件。該條件下,T細胞的活力、增殖能力、TCR編輯效率及幹細胞樣記憶表型均保持穩定,且能誘導代謝重編程——在增強糖酵解依賴的同時保留線粒體功能與備用呼吸能力。
功能學驗證顯示,該組T細胞在低效靶比下體外殺傷能力顯著增強,體內抑瘤效果穩定;RNA測序亦揭示其抗腫瘤促炎通路被特異性激活。1% O₂/5 PSI的過度低氧條件會損害T細胞功能(擴增下降、線粒體功能受損、IFN-γ通路下調),無法實現有效預適應。低氧誘導的CD39高表達可能與耗竭或組織駐留記憶T細胞(TRM)形成有關,需進一步探索。
綜上,本研究提出的T細胞體外類腫瘤微環境預適應馴化策略,為突破實體瘤T細胞治療瓶頸提供了可工業化轉化的新路徑。該策略無需復雜的後續基因改造,僅通過AVATAR系統精準模擬TME核心特征,即可重塑T細胞的代謝與功能表型,在保障臨床製備效率的同時提升其抗腫瘤效能。未來,可通過更貼近臨床的實驗體系進一步驗證該策略的臨床轉化價值,推動其早日應用於實體瘤患者的治療。



