2026.04.02
在新藥研發進程中,藥物性肝損傷(DILI)和胃腸毒性是導致候選藥物研發失敗的核心因素。行業數據顯示:藥物從Ⅰ期臨床到最終獲批上市的成功率僅8%,其中安全性相關問題占研發失敗原因的比例高達59%。傳統毒理學評價依賴動物模型和二維(2D)細胞培養,存在顯著局限:2D 單層細胞會在數天內喪失關鍵代謝功能,易產生假陽性或假陰性結果,既可能誤判安全分子,也可能放行高風險化合物進入臨床。
2025年4月,美國FDA 發布逐步淘汰動物試驗的路線圖,明確將基於人類原代細胞的新方法學(NAMs)從研發中的 「可選補充手段」 升級為藥品監管層面的 「剛需技術」。美國 VivoSim 公司推出 NAMkind™ 毒理學平臺,該平臺依托專利化的人源 3D 肝臟與腸道模型,可有效彌補傳統藥物評價模型的技術局限,為藥物研發提供高度貼合人體生理特征、可靠性強的安全數據,為小分子、抗體藥物偶聯物(ADC)等多模態藥物的管線研發保駕護航,助力優質候選藥物高效推進研發進程。
NAMkind™平臺:體外重構功能性人源肝腸組織,真實還原生理毒性應答
NAMkind™平臺突破傳統動物實驗與簡化細胞體系的技術局限,依托專利多細胞共培養技術,以健康供體來源的人原代肝細胞、腸上皮細胞、平滑肌細胞、成纖維細胞及內皮細胞為原材料,構建出具備完整生理結構與功能的3D微組織模型。該模型可穩定培養7~21天,能精準模擬藥物在人體內的長期暴露模式與聯合用藥場景。
NAMkind™ 肝臟模型:精準捕捉 DILI 風險
NAMkind™肝臟模型采用肝細胞、Kupffer 細胞、肝星狀細胞、內皮細胞四細胞共培養體系,高度還原人體肝臟微環境,可通過炎癥、纖維化等多條通路綜合評估肝毒性。模型以 ATP、LDH、白蛋白為核心檢測標誌物,對 DILI 的預測準確率達 91%、敏感性 88%、特異性 100%,有效排除假陽性結果幹擾,降低後期研發失敗風險。
NAMkind™ 腸道模型:精準評估腸道毒性與部位特異性
NAMkind™腸道模型由人原代腸上皮細胞、平滑肌細胞、成纖維細胞及內皮細胞共培養構建,具備極化上皮結構、緊密連接功能,以及功能性CYP450酶與轉運蛋白體系,可穩定分泌黏蛋白,支持屏障完整性、組織活力等多維度指標檢測,能夠捕捉傳統評價方法難以識別的腹瀉、炎癥等腸道毒性反應。模型提供回腸與結腸專屬版本,可分區監測不同腸段的細胞活力,動態反映藥物對腸道的部位特異性毒性特征,為臨床劑量選擇與風險管理提供關鍵參考數據。
服務模式:貫穿研發全周期,實現毒性風險前置與精準管控
NAMkind™毒理學服務深度匹配藥物研發的核心決策節點,將肝腸毒性風險管控環節前置,覆蓋研發全周期,可提供分階段定製化服務:
1. 前瞻性篩選(Hit-to-Lead 及早期先導優化)
該服務可在2周內完成20余種化合物的篩選,通過核心生物標誌物(ATP、白蛋白、LDH、TEER等)快速識別肝腸毒性信號,為化合物化學結構優化提供方向指導,助力研發團隊鎖定高安全性候選分子。
2. 轉化風險橋接(晚期先導優化→候選物提名)
搭配物種特異性模型與機製研究矩陣,驗證動物實驗數據與人體生理反應的相關性,輸出符合新藥臨床試驗(IND)申報要求的安全性數據,支撐監管申報材料提交。
3. 研究性毒理學(臨床 / 臨床前意外毒性)
可快速重現或排除待確認的毒性信號,深入追溯毒性發生的分子機製,為項目後續推進、優化或終止的決策提供明確建議,高效實現項目價值,避免不必要的研發全線停擺。
技術實力:經臨床藥物驗證,為研發決策提供可靠數據支撐
NAMkind™模型已通過大量經臨床驗證的藥物全面校驗,預測精度優異,不僅適用於小分子藥物的毒性評估,更可對ADC等大分子藥物的肝腸毒性實現精準評價,檢測結果與藥物臨床實際表現高度吻合。
1. 小分子藥物驗證:精準識別結構相似化合物的差異毒性
肝臟模型:因嚴重 DILI 撤市的曲格列酮、曲伐沙星,在模型中均表現出顯著的肝細胞功能抑製,ATP 與白蛋白水平大幅下降;而其同類安全藥物吡格列酮、左氧氟沙星則無明顯毒性信號,該對照結果充分證明模型可精準篩選安全性更優的候選藥物分子。

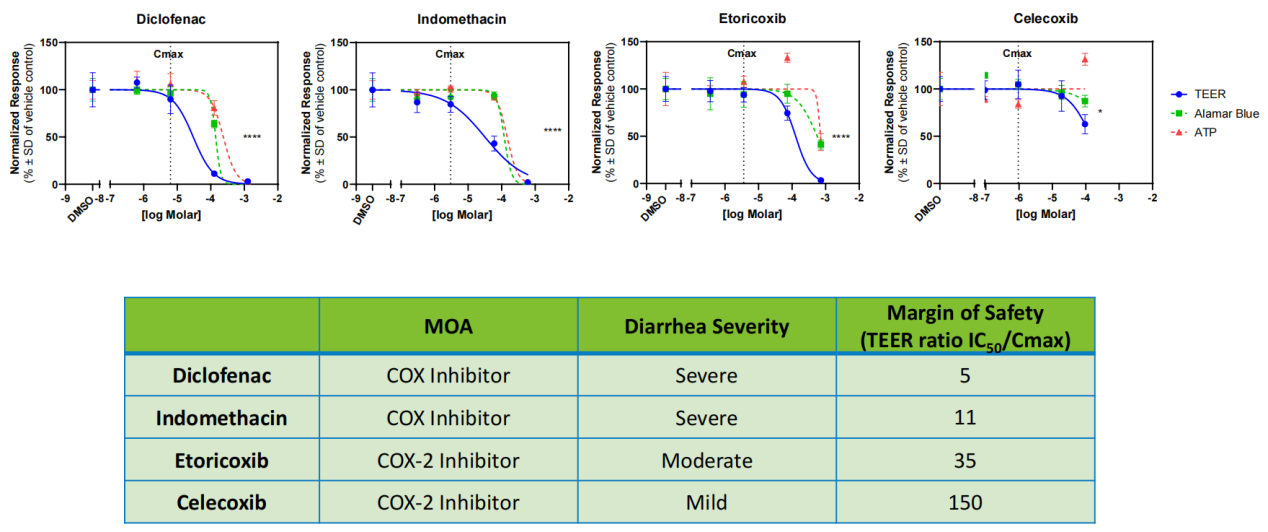
腸道模型:對非甾體抗炎藥的驗證顯示,雙氯芬酸、吲哚美辛的腸道毒性顯著,安全邊際值僅為5倍和11倍;而塞來昔布、依托考昔的毒性輕微,對應安全邊際值分別達150倍和35倍,模型檢測結果與藥物臨床引發的腹瀉嚴重程度高度匹配。
2. ADC藥物驗證:精準區分靶向 / 脫靶毒性,針對性解決 ADC 研發中的核心安全挑戰
肝臟與胃腸道是ADC類藥物主要脫靶毒性器官。NAMkind™模型依托人原代細胞的天然靶點表達特征,可精準解析藥物毒性作用機製。
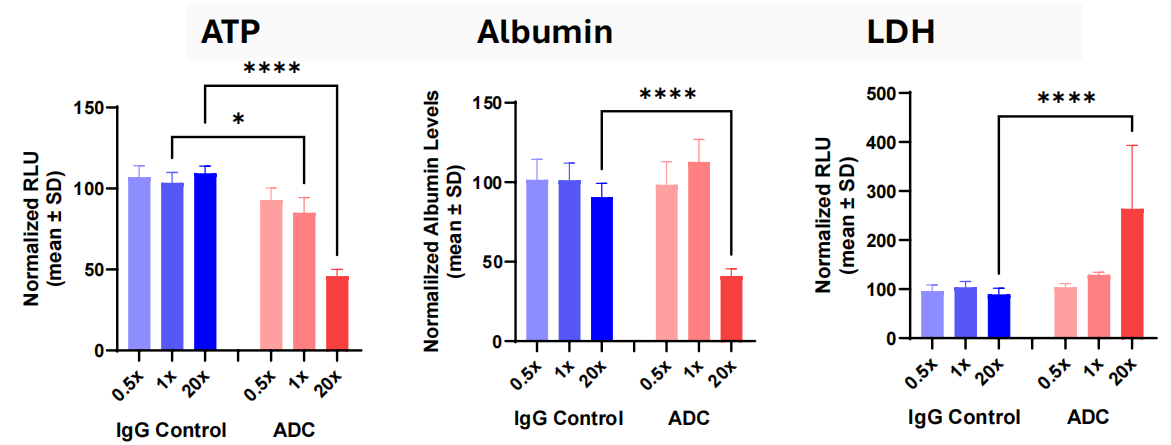
肝臟模型:針對靶向CD33的吉妥珠單抗奧佐米星開展的測試顯示,因模型中內皮細胞與Kupffer細胞高表達CD33,該藥物呈現出顯著的劑量依賴性肝毒性,即ATP 下降、白蛋白分泌受抑和LDH 釋放升高;三項核心肝毒性指標均表現出明顯的劑量依賴性變化,而同亞型對照IgG無任何毒性信號。模型檢測結果與該藥物臨床易引發肝竇阻塞綜合征的肝毒性特征高度吻合,直觀驗證了模型能精準識別 ADC 靶點介導的肝損傷風險。
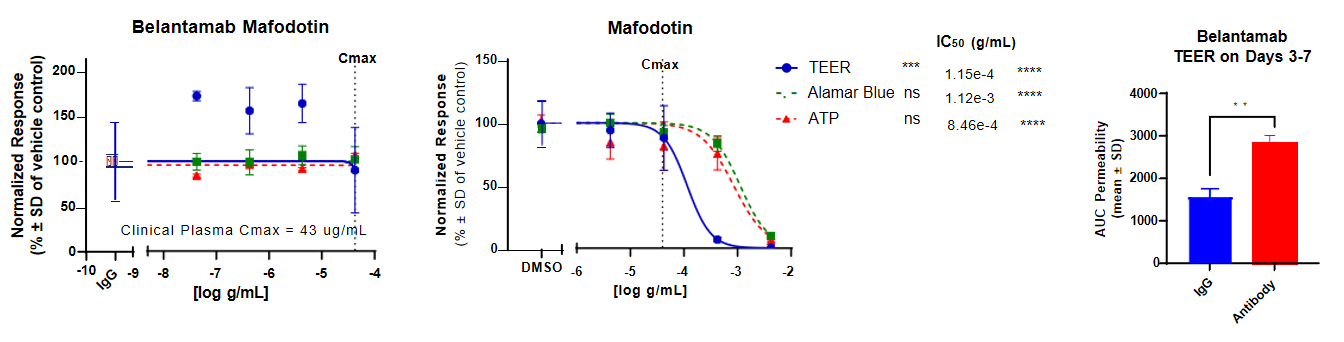
腸道模型:在NAMkind™腸道模型中對靶向HER2的ADC藥物恩美曲妥珠單抗開展驗證,由於模型細胞高表達該藥物的作用靶點HER2,完整ADC在TEER(跨上皮電阻)、Alamar Blue(細胞活力檢測)、ATP(三磷酸腺苷)三項檢測指標上均呈現顯著的劑量依賴性毒性;此外遊離載荷也表現出毒性,未偶聯的抗體單獨作用即可破壞黏膜屏障,整體結果與臨床中該藥物引發腹瀉等胃腸道不良反應高度一致,證實NAMkind™腸道模型可準確識別ADC的靶點介導的胃腸道毒性,適用於ADC早期胃腸道安全風險評估。

核心競爭優勢:高預測精度與高效研發並行,賦能研發價值提升
NAMkind™憑借高精準、快周轉、全合規、多模態的核心優勢,成為藥物毒理學評價的新一代解決方案,相較傳統毒理學模型與同類產品,可為藥物研發創造顯著價值:
優異預測精度:肝臟模型 DILI 預測準確率達91%(特異性 100%)、腸道模型腸道毒性預測準確率達96%(敏感性 97%),可精準捕捉傳統模型遺漏的人體特異性毒性信號;
高效周轉效率:從接收受試化合物到出具完整機製評價報告僅需4周左右,前瞻性篩選僅需2周即可完成,較常規動物實驗(4-6個月)提速數倍,搶占研發窗口期;
大幅降本增效:臨床前篩除 1 個高毒性候選化合物,可避免後期數億美元的研發損失,目標將毒性導致的臨床失敗率降低 50%,性價比遠超動物實驗;
全球監管認可:完全符合FDA NAMs規範,同步適配NMPA、EMA的監管要求,符合國際申報標準,輸出的監管級數據可直接支撐IND申報,有效提升申報成功率;
ADC專項能力:可精準區分ADC靶向/脫靶毒性,解析連接子類型、DAR 值對毒性的影響,針對性解決國內ADC研發面臨的關鍵安全問題,為海外授權與出海提供合規數據支撐;
全流程覆蓋能力:可覆蓋從苗頭化合物篩選、先導化合物優化,到候選化合物(PCC)提名、IND申報,再到臨床階段意外毒性溯源研究的全鏈路環節,可為藥物研發全周期提供定製化毒理學評價服務,實現毒性風險的全流程前置管控。
NAMkind™依托高仿真人源化3D肝腸器官模型,憑借經臨床驗證的高預測精度,直擊藥物研發中肝損傷與腸道毒性兩大核心安全痛點。該平臺不僅填補了傳統動物與細胞模型在人體毒性預測上的技術短板,更以全流程、合規化、高效率的毒理學服務,貫穿藥物從早期篩選到臨床申報的全研發周期。
未來,NAMkind™ 將持續賦為小分子、ADC等多模態創新藥研發賦能,有效降低臨床失敗風險、壓縮研發周期、節約研發成本,助力中國創新藥合規出海、高效落地,推動更多安全可靠的候選藥物早日實現轉化上市。



